近日,国际著名学术期刊《PLoS Genetics》在线发表了王福�教授与闵军霞教授团队合作新成果 “Zebrafish slc30a10 deficiency revealed a novel compensatory mechanism of Atp2c1 in maintaining manganese homeostasis”。该成果利用CRISPR/Cas9技术在斑马鱼中敲除转运膜蛋白slc30a10,首次成功构建人类高锰血症综合征(HMDPC,Hypermanganesemia with dystonia, polycythemia, and cirrhosis)疾病斑马鱼模型;并揭示转运膜蛋白SLC30A10外排锰离子以及与膜蛋白ATP2C1协调维持机体锰离子稳态的分子机制[1]。

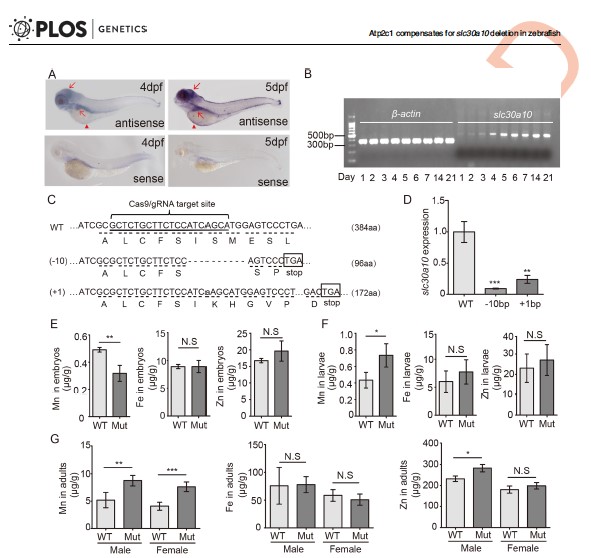
成功制备slc30a10基因敲除斑马鱼并解析锰代谢异常表型
锰元素是人体必需的微量元素,在维持机体正常生理活动与新陈代谢等方面起到了重要作用。例如,锰元素作为生物酶的辅助因子而存在于多种器官、组织以及细胞中,其广泛参与体内碳水化合物、氨基酸和脂质的代谢过程,并且在神经传导、骨骼与结缔组织生长、免疫反应和血液凝结等方面发挥作用[2]。然而,人类对于锰离子代谢的精密调控知之甚少。近年来,由于锰离子转运蛋白突变而造成稳态代谢紊乱的遗传疾病正在被科学家们渐渐揭开神秘的面纱。锰离子代谢已成为当今的一个研究热点。
两个研究组2012年在《American Journal of Human Genetics》同期报道了SLC30A1突变引发HMDPC 疾病(OMIM #613280),其典型病理症状为由于体内锰离子过量蓄积而导致的肌张力失常、运动失调、红细胞增多以及肝脏脂肪化和肝硬化,并提示该基因可能转运锰离子[3,4]。通过外显子测序发现,患者由于发生SLC30A10纯合突变(包括移码突变、无义突变和错义突变等多种形式)缺失了保守的氨基酸,导致体内锰离子过量蓄积,从而诱发HMDPC疾病。迄今为止,已经报道28例HMDPC疾病病例[5]。
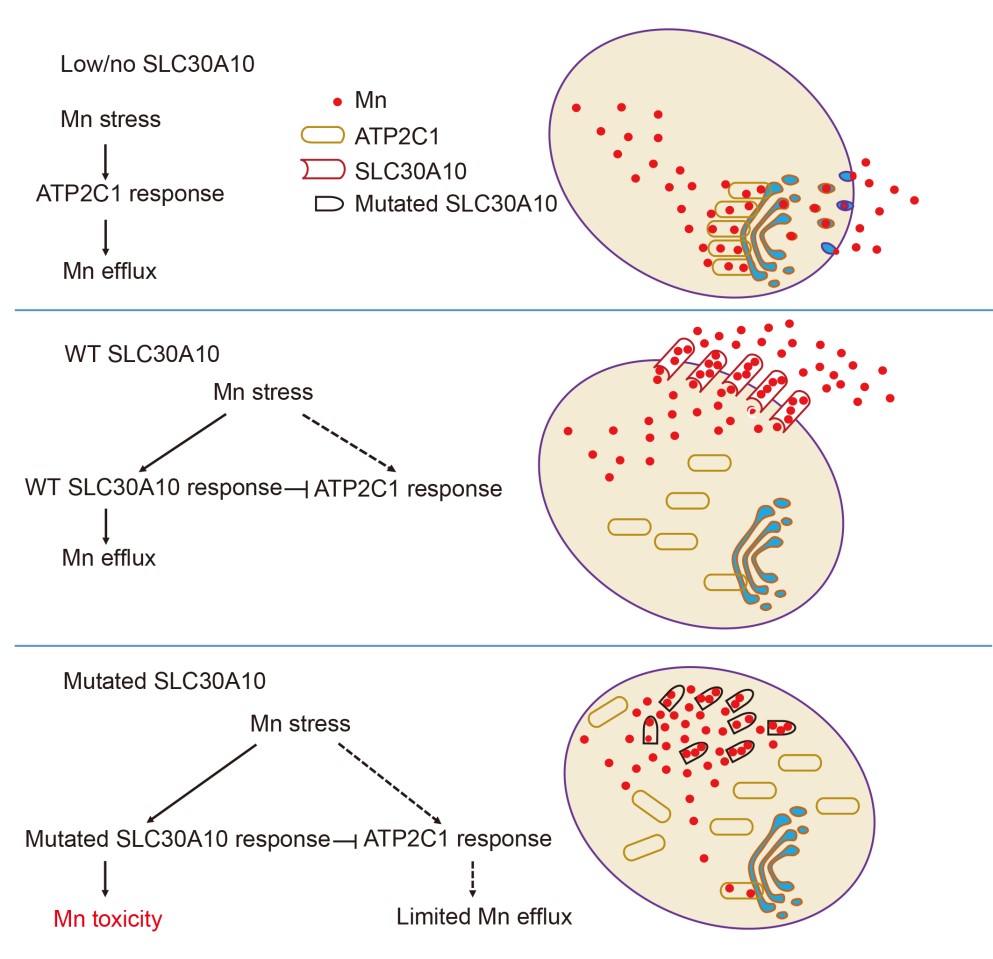
膜蛋白SLC30A10与ATP2C1协作维持细胞锰离子稳态模式图
在王福�和闵军霞教授的共同指导下,夏�丹博士(讲师)和博士生魏家�利用CRISPR/Cas9技术构建了slc30a10突变型(功能缺失)斑马鱼品系,并系统考察了突变体中锰离子蓄积水平、神经元损伤、运动能力、肝脏结构和功能、红细胞数量等生理指标。实验发现突变体斑马鱼的表型与人类HMDPC疾病的病理特征极为相似,为突变型斑马鱼作为疾病模型奠定了科学基础。通过斑马鱼模型以及细胞培养模型共同确认了在SLC30A10缺失或表达量较低的情况下,锰离子会通过介导其囊泡转运蛋白ATP2C1排出;然而,无论是野生型还是突变型SLC30A10启动表达时,囊泡途径会部分受到抑制。锰离子蓄积在突变体细胞内从而造成毒性,导致系统性疾病的发生。
该成果是在国际上首次成功建立HMDPC疾病的斑马鱼人类疾病模型,为药物筛选以及深入机制研究提供了珍贵实验工具;同时,揭示了膜蛋白SLC30A10外排锰离子以及与膜蛋白ATP2C1协调维持机体锰离子稳态的精密分子机制。该成果丰富了锰离子稳态代谢理论,为HMDPC等重大疾病防治提供了重要科学依据。该工作为云顶集团yd1233公共卫生学院和转化医学研究院联合完成。王福�教授与闵军霞教授为本研究的共同通讯作者。该工作得到国家自然科学基金委经费支持。
参考文献:
[1] Zhidan Xia, Jiayu Wei, Yingniang Li, Jia Wang, Wenwen Li, Kai Wang, Xiaoli Hong, Lu Zhao, Caiyong Chen, Junxia Min, Fudi Wang. (2017) Zebrafish slc30a10 deficiency revealed a novel compensatory mechanism of Atp2c1 in maintaining manganese homeostasis. PLoS Genetics 13(7): e1006892. https://doi.org/10.1371/journal.pgen.1006892
[2] Aschner M et al. (2007) Manganese: recent advances in understanding its transport and neurotoxicity. Toxicol Appl Pharmacol, 221(2):131-147.
[3] Quadri M et al. (2012) Mutations in SLC30A10 cause parkinsonism and dystonia with hypermanganesemia, polycythemia, and chronic liver disease. Am J Hum Genet, 90(3):467-477.
[4] Tuschl K et al. (2012) Syndrome of hepatic cirrhosis, dystonia, polycythemia, and hypermanganesemia caused by mutations in SLC30A10, a manganese transporter in man. Am J Hum Genet, 90(3):457-466.
[5] Quadri M et al. (2015) Manganese transport disorder: novel SLC30A10 mutations and early phenotypes. Mov Disord 30: 996-1001.


